Lainsäädäntö, lääkealan laatustandardit ja viranomaiset varmistavat lääkkeiden tuotantoprosessien ja lopputuotteiden laadukkuuden. Laatuun on aina voinut luottaa ja voi edelleen. Valmistuspaikkatiedolla on kuitenkin arvoa.
Lääke valmistetaan vaaditut kriteerit täyttävistä raaka-aineista, jotka on määritelty myyntilupadokumentaatiossa. Lääkkeen tärkein raaka-aine on lääkeaine eli aktiiviaine. Aktiiviaine tekee lääkkeestä lääkkeen. Siitä käytetään usein myös englanninkielistä lyhennettä API (Active Pharmaceutical Ingredient). Niitä ovat esimerkiksi ibuprofeeni, parasetamoli ja rosuvastatiini.
Aktiiviaineesta valmiiksi lääkkeeksi
Lääkkeen valmistus alkaa aktiiviaineen tuotannosta. Niitä valmistetaan aktiiviaineiden valmistukseen erikoistuneissa tehtaissa. Valmistukseen tarvitaan raaka-aineita ja valmistus tapahtuu myyntiluvassa esitetyn prosessin mukaisesti. Lähtöaineet ja lopputuote analysoidaan.
Myyntiluvassa voi olla rekisteröitynä useita valmistajia samalle aktiiviaineelle. Tämä tuo joustoa lääkkeen tuotantoprosessiin ja vähentää saatavuusriskejä. Hyväksyttynä voi olla esimerkiksi omassa tuotannossa valmistettava aktiiviaine ja yksi tai kaksi yhteistyökumppanien valmistamaa lääkeainetta. Aktiiviaineen tuotantopaikat ja valmistusmaat voivat vaihdella tuotantoerittäin.
Seuraava valmistusvaihe on lääkkeen valmistus (bulkkituotanto). Tabletit, kapselit ja liuokset valmistetaan lääkeaineesta ja määritellyistä apuaineista. Raaka-aineiden laatu varmistetaan ennen tuotantoprosessia.
Viimeinen tuotantovaihe on pakkaaminen: esimerkiksi tabletit pakataan läpipainopakkauksiin tai purkkeihin, suojaksi tulee usein myös pahvikotelo ja mukaan lisätään potilasohje. Lopuksi lääke vielä analysoidaan ja vapautetaan myyntiin.
Miten määritellä lääkkeen valmistusmaa?
Lääkkeen raaka-aineet voivat tulla ja tulevatkin usein useasta eri maasta ja usein myös Euroopan ulkopuolelta – esimerkiksi Aasiasta. Euroopassa on kuitenkin vielä esimerkiksi aktiiviaineiden tuotantoa.
Valmistusmaan määrittely raaka-aineiden perusteella ei ole yksiselitteistä. Melko tavallista on määritellä valmistusmaa lääkkeen valmistuspaikan (bulkkituotanto) perusteella. Omassa luokittelussamme noudatamme tätä käytäntöä. Pakkaaminen voidaan tehdä muualla, mutta varsin usein se tehdään valmistavassa tehtaassa tai lääketehtaassa sen lähistöllä.
Euroopassa myydyn lääkkeen laadusta vastaa aina eurooppalainen lääketehdas. Tämä koskee myös kaikkia Euroopan ulkopuolella valmistettuja lääkkeitä. Jokainen Eurooppaan saapuva lääke-erä analysoidaan ja vapautetaan erikseen myyntiin.
Vapautuksen tekevä lääketehdas näkyy pakkausselosteessa valmistajana. Vapautus varmistaa lääkkeen laadun, mutta voi antaa harhaanjohtavan kuva lääkkeen valmistuspaikasta. Merkintätavan perusteella voisi tulkita, että kaikki Euroopassa myytävät lääkkeet on valmistettu Euroopassa. Näin ei kuitenkaan ole.
Tevalla on laaja eurooppalainen tehdasverkosto
Tevalla on laaja eurooppalainen tuotantolaitosten verkosto. Tabletit, kapselit ja liuokset valmistetaan, analysoidaan ja pakataan lähellä eurooppalaisia lääkkeiden tarvitsijoita. Kuljetusmatkat ovat verrattain lyhyet.
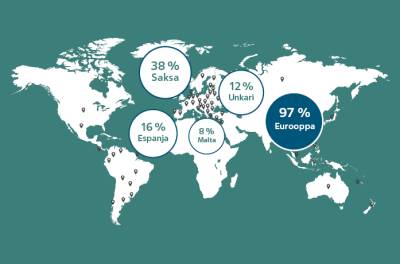
Suomessa myymistämme pakkauksista valtaosa (97 %) valmistetaan Euroopassa. Tämä prosenttiosuus on viime vuosina kasvanut. Olemme siirtäneet tuotantoa Eurooppaan muun muassa Israelista ja Intiasta. Suurin osa myymistämme lääkkeistä valmistetaan Saksassa ja toiseksi suurin osa Unkarissa – seuraavat suuruusjärjestyksessä ovat Espanja ja Malta. Valmistusmaiden osuuksia on havainnollistettu taulukossa yksi.